高中化学:原电池、电解池、电镀池的比较
1、原电池、电解池、电镀池的比较

2、电解电极产物的判断
要判断电极反应的产物,必须掌握离子的放电顺序,判断电极反应的一般规律是:
(1)在阳极上
①活性材料作电极时,金属在阳极失电子被氧化成阳离子进入溶液,阴离子不容易在电极上放电。
②用惰性电极(Pt、Au、石墨、钛等)时;溶液中阴离子的放电顺序是:

(2)在阴极上
无论是惰性电极还是活性电极都不参与电极反应,发生反应的是溶液中的阳离子,阳离子在阴极上放电顺序是

3、金属的腐蚀

例1、如图所示,请按要求回答下列问题。

(1)打开

,合并

。
A为(填“正”或“负”)________极,在该电极可观察到的现象是________________;B极的电极反应为________________________。
(2)打开

,合并

。
A为(填“阴”或“阳”)________极,在该电极可观察到的现象是________________;B极的电极反应为________________;当有0.2mol电子转移时,则析出铜的质量为________g。
答案:(1)负 A处金属不断溶解

(2)阴 A上有红色金属析出

6.4
分析:打开

,合并

,该电池为原电池,A为负极,电解反应为:

,B极为正极,正极反应为:

。打开

,合并

,则构成了电解池,A为阴极,电解反应为:

,B极为阳极,阳极反应为:

。
例2、水银法电解食盐水是氯碱工业发展进程中的重要里程碑,以制得碱液纯度高、质量好著称,其生产原理示意如下:

(1)分别写出电解池、解汞室中发生反应的离子方程式。
(2)当阳极产生

(标准状况)

时,解汞室中生成

的质量为多少千克?
(3)电解室中

溶液的流入、流出速率均为
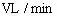
,若生产上要求流出碱液的物质的量浓度为

,计算解汞室中碱液的流出速率Q(单位:

)。
(4)20世纪60年代,氯碱生产采用离子膜法,水银法逐渐被淘汰,你认为被淘汰的主要原因是什么?
分析:首先分析出电解池、解汞室中发生反应的离子方程式分别为:

和

,根据这两个方程式就可以计算出生成的氢氧化钠的质量。根据方程式还可以发现消耗的

的物质的量和生成的氢氧化钠的物质的量相等。据此,可以列出方程:

。
答案:(1)电解池:

解汞室:

(2)解:


(3)Q=

(4)汞有毒性,对环境造成污染。
例3、常温下电解

一定浓度的

与

混合溶液,理论上两极所得气体的体积随时间变化的关系如图I、II所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:

(1)原混合溶液

和

的物质的量浓度。
(2)

时所得溶液的

。
(3)电解至

时,消耗水的质量。
答案:(1)阳极首先逸出的是氯|气:

,则
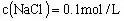
,阳极得到

气体中,含


和


,转移电子的物质的量为:

,此过程中阴极刚好全部析出铜:

,则

。
(2)

时溶液中

,

,根据电荷守恒有:

,即溶液的

。
(3)电解至

时,消耗水
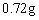
,在电解的过程中,两极依次发生的反应为:

电解的过程,首先是电解氯化铜,进而是电解硫酸铜溶液,最后是电解水。
-
上一篇:高一化学必修二期末复习提纲